がん抑制タンパク質を分解誘導するE3リガーゼの同定
Discovery of E3 ligase degradating tumor-suppressor protein
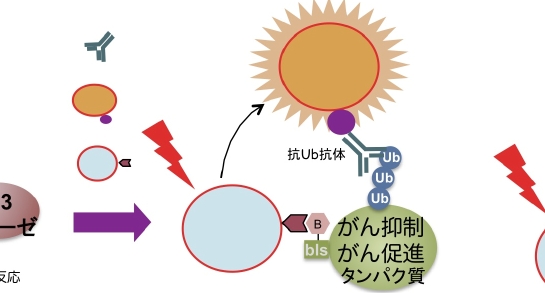
コムギ無細胞系はユビキチン化タンパク質研究に適している
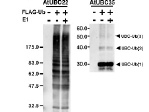 ポリユビキチン鎖を作製可能リン酸化、メチル化、糖鎖付加など、様々なタンパク質の翻訳後修飾が知られていますが、その中でもユビキチン化は最もタンパク質の機能を多様化させる翻訳後修飾かもしれません。しかし、細胞内には数分以内にタンパク質を完全に分解できるプロテアソームがあるため、遺伝子導入を行うとユビキチン化されたタンパク質や、E3リガーゼは自己ユビキチン化反応により分解されてします。そのため、細胞を用いてユビキチン化行うことは難しいのが現状です。コムギ無細胞系はプロテアソームを含んでいないため、分解シグナルのK48ポリユビキチン鎖が付加されたタンパク質も安定です。これは、ユビキチン化タンパク質の機能解析を行う上で、非常に有利な点となっています。
ポリユビキチン鎖を作製可能リン酸化、メチル化、糖鎖付加など、様々なタンパク質の翻訳後修飾が知られていますが、その中でもユビキチン化は最もタンパク質の機能を多様化させる翻訳後修飾かもしれません。しかし、細胞内には数分以内にタンパク質を完全に分解できるプロテアソームがあるため、遺伝子導入を行うとユビキチン化されたタンパク質や、E3リガーゼは自己ユビキチン化反応により分解されてします。そのため、細胞を用いてユビキチン化行うことは難しいのが現状です。コムギ無細胞系はプロテアソームを含んでいないため、分解シグナルのK48ポリユビキチン鎖が付加されたタンパク質も安定です。これは、ユビキチン化タンパク質の機能解析を行う上で、非常に有利な点となっています。
がん抑制タンパク質を分解誘導するE3リガーゼの探索・同定
 ユビキチン化システムがん抑制タンパク質が正しく機能していると、ほとんどの場合、細胞のがん化を強力に抑制することができます。がん細胞の多くでは、これらがん抑制タンパク質の機能不全が起こっています。最近、がん細胞の中には、がん抑制タンパク質がユビキチン化され直ちに分解している例があることがわかってきました。特定にE3リガーゼががん抑制タンパク質を分解誘導していたのです。そこで我々は、コムギ無細胞系の利点を活かして、がん抑制タンパク質を分解誘導するE3リガーゼの探索・同定を行っています。将来、新たなに見つかるE3リガーゼが抗ガン剤の標的となるかも知れません。
ユビキチン化システムがん抑制タンパク質が正しく機能していると、ほとんどの場合、細胞のがん化を強力に抑制することができます。がん細胞の多くでは、これらがん抑制タンパク質の機能不全が起こっています。最近、がん細胞の中には、がん抑制タンパク質がユビキチン化され直ちに分解している例があることがわかってきました。特定にE3リガーゼががん抑制タンパク質を分解誘導していたのです。そこで我々は、コムギ無細胞系の利点を活かして、がん抑制タンパク質を分解誘導するE3リガーゼの探索・同定を行っています。将来、新たなに見つかるE3リガーゼが抗ガン剤の標的となるかも知れません。
がん患者特異的自己抗原タンパク質の同定
Discovery of cancer-specific autoantigens inducing in cancer patients
がん患者の血清中には特異的な自己抗体が誘導されることがある
 乳がん自己抗原プロファイリング最近の知見では、ある割合のがん患者血清中に自己抗体が誘導される例があることがわかってきました。我々はこれまでに、自己抗体探索に適したタンパク質ライブラリーを構築してきたので、がん患者血清中の抗体と反応するタンパク質を網羅的に同定してきました。その結果、乳がん患者血清や前立腺がん患者血清中に、種々のがん特異的に誘導される自己抗体を見つけました。これらを上手く用いれば、乳がんや前立腺がんの診断マーカーになる可能性を期待しています。現在、より大規模な形で評価しています。
乳がん自己抗原プロファイリング最近の知見では、ある割合のがん患者血清中に自己抗体が誘導される例があることがわかってきました。我々はこれまでに、自己抗体探索に適したタンパク質ライブラリーを構築してきたので、がん患者血清中の抗体と反応するタンパク質を網羅的に同定してきました。その結果、乳がん患者血清や前立腺がん患者血清中に、種々のがん特異的に誘導される自己抗体を見つけました。これらを上手く用いれば、乳がんや前立腺がんの診断マーカーになる可能性を期待しています。現在、より大規模な形で評価しています。
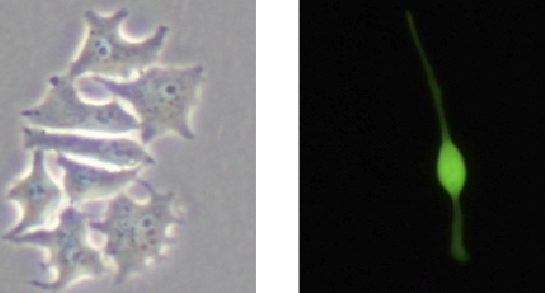
がん特異的自己抗原の中には細胞増殖に関与するタンパク質がある
 細胞増殖に対する自己抗原発現抑制の影響p53という非常に有名ながん抑制タンパク質に対する抗体(抗p53自己抗体)が、がん患者の血清中に誘導されます。我々が見つけた自己抗原タンパク質もp53と同様に,細胞のがん化に関与している可能性を考え調べてみたところ、いくつかの自己抗原タンパク質は、ある種のがん細胞株で発現量が高く、それらの自己抗原タンパク質の発現を抑制すると、がん細胞株の増殖が停止します。がん特異的自己抗原タンパク質は、ひょっとするがん促進タンパク質かも知れません。
細胞増殖に対する自己抗原発現抑制の影響p53という非常に有名ながん抑制タンパク質に対する抗体(抗p53自己抗体)が、がん患者の血清中に誘導されます。我々が見つけた自己抗原タンパク質もp53と同様に,細胞のがん化に関与している可能性を考え調べてみたところ、いくつかの自己抗原タンパク質は、ある種のがん細胞株で発現量が高く、それらの自己抗原タンパク質の発現を抑制すると、がん細胞株の増殖が停止します。がん特異的自己抗原タンパク質は、ひょっとするがん促進タンパク質かも知れません。

 HOME
HOME Cell-free tech
Cell-free tech Research
Research Paper outline
Paper outline Member
Member Publication
Publication Funds
Funds Contact us
Contact us Link
Link Photo
Photo 講義用資料
講義用資料







