Koshiba R, Chisuga T, Fujinami D, Takeda H, Nakano S.
Screening and Engineering of Ancestral Sortase Es That Enable High-Fidelity Enzyme Design with Activity Trade-Off.
Bioconjug Chem. 2026 Jan 27.
doi: 10.1021/acs.bioconjchem.5c00576.
PMID: 41589451.
このたび、静岡県立大学の中野祥吾先生との共同研究の成果が、米国化学会の学術誌『Bioconjugate Chemistry』に掲載されました。
【論文紹介】活性とのトレードオフで実現する「高忠実度」な祖先型ソルターゼEの開発
近年、抗体医薬品の製造や機能性材料の開発において、異なるタンパク質同士を連結させる技術(タンパク質ライゲーション)が非常に重要になっています。 私たちの研究チームは、この連結反応を触媒する酵素「ソルターゼ(Sortase)」に着目し、より精密で副反応の少ない新しい酵素の開発に成功しました。タンパク質の連結には、一般的に「ソルターゼA(Sortase A)」という酵素がよく使われますが、反応性が低かったり、意図しない副反応(加水分解など)が起きたりするという課題がありました。 以前の研究で、私たちのグループは「祖先配列復元(ASR)」という手法を用いて、非常に活性の高いソルターゼE変異体「AcSE5」を開発しました。しかし、より精密な合成を行うためには、活性だけでなく「基質特異性(狙った相手とだけ反応する能力)」をさらに高める必要がありました。
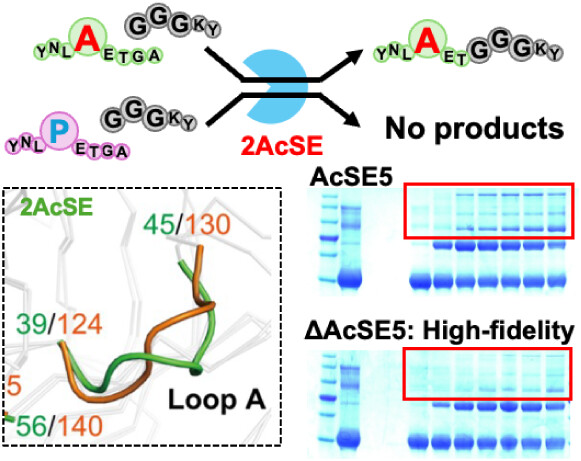
そこで今回、私たちはデータベース上に眠る膨大な未解析配列の中から、理想的な性質を持つ酵素を探し出すことにしました。 約3,000もの配列データを解析・クラスタリングし、コンピュータ上で8種類の「祖先型ソルターゼE(1AcSE〜8AcSE)」を設計しました。実際にこれらを作製して実験を行ったところ、2AcSEという変異体が非常に高い基質特異性を持っていることを発見しました。2AcSEが持つ高い特異性の理由を解明するために構造解析を行った結果、基質結合に関わるLoop Aという領域が非常に短いことを見出しました。この発見をもとに、以前開発した高活性な「AcSE5」に今回発見した「2AcSE」の短いLoop Aを移植したキメラ酵素「ΔAcSE5」を設計しました。ΔAcSE5は、元の酵素に比べて活性自体は低下しましたが、副反応を劇的に抑え、目的のタンパク質結合のみを正確に行う高い特異性を獲得しました。
本研究は、新規配列の特性と構造に基づいた合理的な設計により新たな酵素デザインを提案しました。 この成果は、より高品質な次世代抗体医薬品の製造や、精密なバイオマテリアルの合成への貢献が期待されます。

